はじめに
身の回りの様々な場所で利用されている「火」ですが、中ではとても面白い現象が起きています。
専門的には火炎と呼ばれる火の中でも、今回の記事では着火反応に絞って、ざっくりと解説します。

火炎と着火
普通の環境の場合、火炎は燃料と酸化剤が混ざった場所に着火源をもっていくと発生します。
家のガスコンロで考えてみましょう。まずツマミをひねるとガスが出て周りの空気と混ざります。
そして、ツマミを回しきると電気を使った火花が飛んで、それを着火源として火炎が形成します。
着火する前までは単なる燃料と空気の静かな流れだったのに、いったん火が付けば、高温のガスと光が瞬く間に発生します。着火という現象を挟むと、別人のように状態が変わってしまうのです。
ちなみに高校で化学を選択した方であれば、燃焼は酸化反応であり、主に下記のような化学反応式であらわされることを知っているかと思います。
\(\rm{CH}_4+\rm{2O}_2→\rm{CO}_2+\rm{2H}_2\rm{O}\)
これはメタンと酸素の反応を表す式です。都市ガス中の約90%がメタンなので、上で示した例では大部分でまさにこの反応が起きていることになります。
この式は、燃料が完全に燃焼していれば、メタン1に対して酸素が2の割合で消費されて、二酸化炭素と水が1:2の割合で生成することを意味しています。
つまり、火炎前後の変化をひとまとめにした式なのです。
したがって、着火のダイナミックな変化は、この式からは読み取ることはできません。
では、実際の火炎の中はどうなっているのでしょうか?
結論から言うと、火炎の中では急速な化学反応が、たくさん発生しまくっています。
火炎の中の化学反応
火炎の中をより詳細に調べた結果、メタンと酸素の燃焼では約80個もの化学反応が起きていることがわかっています。その一部1を下に示します。
いきなりたくさんの式が出てきてびっくりしてしまいますが、今回は着火に絞って式のつながりを見てみましょう。
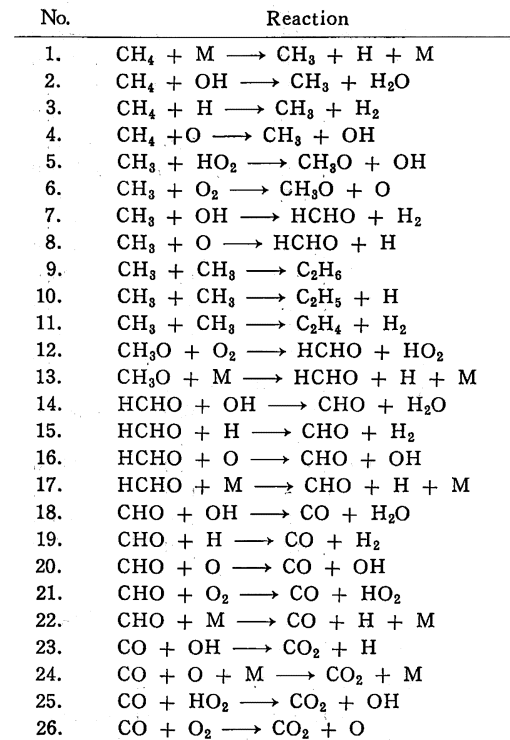
まず、見慣れないMについて説明します。これは第3体と呼ばれていて、反応中にある何の分子でもよいということを表しています。例えば式1でいけば、Mの部分はOHでもCOでも何でもよくて、とりあえず何らかの分子とメタンが反応することで、CH4がCH3とHに分裂することを意味します。
(ただしこの反応は反応に必要なエネルギーが大きいので、普通にしていたら反応は起きません)
\(\rm{CH}_4+\rm{M}→\rm{CH}_3+\rm{H}+\rm{M}\)
これを踏まえて式を見ると、式1~4でCH3と書かれた分子が生成していることがわかります。
この分子はメタンからHが1つ欠けた形をしていて、状態としては不安定です。
不安定ということは、相方が見つかればすぐ反応して安定状態に戻りたがるので、とても反応しやすい分子であることを意味します。
このような原子や分子をラジカルと呼び、中でもCH3はメチルラジカルと呼ばれています。
メチルラジカルは式6で酸素と反応して、Oラジカルを生成します。
そしてこのOラジカルは式4でメタンと反応し、さらにメチルラジカルとOHラジカルを生成します。OHラジカルも式2でメチルラジカルを生成するので、連鎖的にラジカルが増えていくことになります。
\(\rm{CH}_3+\rm{O}_2→\rm{CH}_3\rm{O}+\rm{O}\)
\(\rm{CH}_4+\rm{O}→\rm{CH}_3+\rm{OH}\)
\(\rm{CH}_4+\rm{OH}→\rm{CH}_3+\rm{H}_2\rm{O}\)
このように燃焼反応では、ラジカルを橋渡しとして連鎖的に反応が進行していきます。これによってメタンは急速に分解されて、やがては着火に至ります。
ちなみに、式1~4のような初期のラジカル生成を起こすためには一定のエネルギーが必要です。
電気火花の場合は局所的には数千度になることもあるので、反応を引き起こすことができます。
さいごに
いかがでしたでしょうか。
今回は火炎の中の化学反応、特に着火反応に絞って解説を行いました。
燃焼の分類としては、流れとの関係性も重要となるので、そちらは別の機会にまとめていこうと思います。
本格的に勉強したい方は以下の参考文献を読んでみてください。
参考論文
- S. Fukutani, H. Jinno, “Dynamics of Reactive Systems Part 1 : Flames and Configurations”, eded by J. R. Bowen, J. C. Leyer, R. I. Soloukhin, The American Institute of Aeronautics and Astronautics (1986) p. 263. ↩︎





コメント